Richtlijnen
Format richtlijnontwikkeling voor SWAB richtlijnen
Onderstaande procedure voor richtlijnontwikkeling is voorgesteld door de commissie richtlijnen van de SWAB, en wordt door deze commissie geëvalueerd en zo nodig aangepast. Onderstaande versie is goedgekeurd door het SWAB bestuur op 4 februari 2021.
Inhoud
De SWAB richtlijnen betreffen aanbevelingen met betrekking tot antimicrobiële therapie en profylaxe. Principes van diagnostiek worden opgenomen voor zover zij essentieel zijn voor het beleid. De omvang van dit deel kan per richtlijn verschillen. Het is niet de bedoeling om uitgebreide diagnostiekrichtlijnen te maken. De SWAB richtlijnen verschillen hierin van de richtlijnen van specialistenverenigingen (NVALT e.d.), die vaak betrekking hebben op andere aspecten van de behandeling van een infectie.
Doelgroep
Het programma richtlijnen is gericht op intramuraal gebruik van antimicrobiële middelen in ziekenhuizen. De doelgroep bestaat uit de antibioticacommissies van ziekenhuizen die met hulp van de SWAB richtlijnen lokale protocollen (antibioticaboekjes) opstellen. De SWAB beheert een geactualiseerd adresbestand van de antibiotica/geneesmiddelencommissies. De SWAB richtlijnen verschillen hierin van de richtlijnen van specialistenverenigingen, die zich richten tot individuele voorschrijvers.
Er wordt naar gestreefd ook bij te dragen aan de ontwikkeling van richtlijnen voor extramuraal/eerstelijns antibioticagebruik. Er is daartoe een convenant met het Nederlands Huisartsen Genootschap (NHG). Bij het ontwikkelen van SWAB-richtlijnen zal het NHG uitgenodigd worden een lid af te vaardigen naar de commissie die een specifieke richtlijn voorbereidt. Anderzijds zegt de SWAB toe waar nodig bij te dragen aan (herziening van) NHG standaarden. Ook wordt indien aan de orde afgestemd met Verenso, de vereniging van specialisten Ouderengeneeskunde, met zo nodig afgevaardigden in elkaars richtlijnen.
Format Richtlijnontwikkeling
- Het onderwerp voor de richtlijnen wordt door de commissie richtlijnen na inventarisatie via een SWAB bestuursvergadering aangebracht. Er wordt een voorzitter aangeduid als eindverantwoordelijke. Er wordt een coördinator aangesteld met subsidiegeld.
De voorzitter stelt (in overleg met het bestuur) een voorbereidingscommissie samen van experts op gebied van infectieziekten, medische microbiologie en ziekenhuisfarmacie (de verenigingen NVII, NVMM en NVZA) die gemandateerd zijn door genoemde verenigingen. Namens deze verenigingen worden ten minste 1, en zo mogelijk 2 leden gemandateerd. In deze fase worden ook de besturen van de beroepsverenigingen waarvoor de richtlijnen bedoeld zijn aangeschreven met de vraag tenminste één gemandateerd lid af te vaardigen namens hun vereniging. Uitdrukkelijk wordt bij elke richtlijn gekeken of participatie van kinderartsen gewenst is. Deze voorbereidingscommissie bestaat dan uit 6-12 personen. - Tijdens een eerste bijeenkomst stelt de voorbereidingscommissie een aantal uitgangsvragen. Deze vraagstellingen zijn afhankelijk van de behoefte uit het veld en de haalbaarheid. Het kan daartoe zinvol zijn om een knelpuntanalyse te verrichten om de vraagstellingen die in het veld leven te inventariseren. Op basis hiervan voert de coördinator een systematische literatuursearch uit.
- Per uitgangsvraag wordt door de coördinator een zoekstrategie ontwikkeld. Combinaties van verschillende voor de vraag relevante sleutelwoorden worden ingevoerd in verschillende literatuur zoekprogramma’s. Hierbij wordt gebruik gemaakt van Medline, Pubmed en de Cochrane Library. Daarnaast wordt – indien relevant voor de betreffende richtlijn - gebruik gemaakt van richtlijnen uit vergelijkbare landen. Wanneer hiervoor de mogelijkheid bestaat kan ook met andere “engines” gezocht worden.
De coördinator screent alle zoekresultaten op titel en abstract en beslist of een artikel relevant, mogelijk relevant of irrelevant is voor het beantwoorden van de betreffende onderzoeksvraag. Alle artikelen uit de eerste en tweede categorie worden opgezocht. Deze volledige tekst van elk artikel wordt preferentieel door twee experts (bijv. coördinator en voorzitter) beoordeeld op relevantie. Hiervoor kunnen voor de individuele onderzoeksvraag relevante checklists gebruikt worden. De als relevant beschouwde artikelen worden dan –eventueel aangevuld door toegevoegde secundaire referenties- samengevat in een tekst waarin wordt gepoogd een antwoord te formuleren op de (vooraf bepaalde) onderzoeksvraag of -subvragen.
In de oudere SWAB Richtlijnen werd een duidelijke gradatie in bewijskracht aangegeven zoals gedefinieerd volgens de CBO – handleiding (mate van bewijskracht -zie CBO handleiding p.21-22).1
Bij de nieuwe SWAB richtlijnen wordt het AGREE instrument gebruikt,2 en volgt de commissie daarnaast een richtlijn-ontwikkelproces vergelijkbaar met dat van de Infectious Diseases Society of America (IDSA), die een systematische methode hanteert om de kwaliteit van de evidence (very low, low, moderate, and high) en de sterkte van de aanbevelingen (weak or strong) te graderen (Figuur 1).3
De kwaliteit van het bewijs wordt gegradeerd volgens het GRADE (Grading of Recommendations Assessment, Development and Evaluation) systeem. Kwaliteit van bewijs wordt door meerdere factoren bepaald, waarvan de belangrijkste het study design is (Fig. 1)4. De overige factoren (bijv. risk of bias) kunnen de kwaliteit van het design versterken of verzwakken.
In de volgende stap worden Aanbevelingen gemaakt, gegradeerd als Strong of Weak. Dit wordt bepaald door kwaliteit van bewijs, patiëntenpreferenties, middelen en kosten, en de balans tussen voordelen en belasting (Fig. 1)5.
De SWAB is van mening dat lage kwaliteit van bewijs niet automatisch resulteert in een zwakke aanbeveling – en omgekeerd. Bijvoorbeeld: afnemen van bloedkweken voor start antibiotica: zwak bewijs, sterke aanbeveling.3,6 Dit wordt bij elke aanbeveling besproken in de sectie: “Overige overwegingen”, zo mogelijk onderscheiden in patiëntenpreferenties, middelen en kosten, en de balans tussen voordelen en belasting.
Als er geen wetenschappelijk bewijs is, worden aanbevelingen gemaakt op grond van de mening en ervaring van de commissieleden, en als zodanig gegradeerd: Expert opinion of Good practice statement (GPS).
Op basis van de systematische literatuur review, de gradering van het bewijs en de overige overwegingen stelt de voorbereidingscommissie aanbevelingen en een conceptrichtlijn op. De (concept)richtlijn wordt in het Nederlands opgesteld; wel wordt een Engelse vertaling van de aanbevelingen in de (concept)richtlijn opgenomen. Ook worden in de tabellen met bewijs (evidence tables) de resultaten van individuele studies in het Engels weergegeven om zo onnodige vertaling te voorkomen. De voorbereidingscommissie kan besluiten, als dit opportuun lijkt, de gehele richtlijn in het Engels op te stellen. Dit besluit moet bekrachtigd worden door de commissie Richtlijnen van de SWAB.
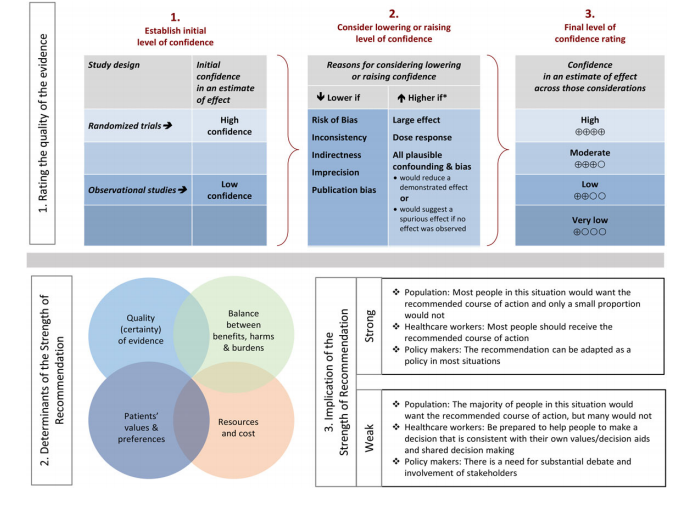
Figuur 1
- Voor een aantal onderdelen van de richtlijn zijn standaard formuleringen opgesteld, weergegeven in bijlage 2. Hierin worden de rol van de SWAB, de scope van de richtlijn (patiëntenpopulatie en aandoeningen), de methodologie, de implementatie, de rol van de sponsor, potentiële conflicterende belangen en de geldigheidsduur van de richtlijn beschreven.
- De conceptrichtlijn wordt via de respectievelijke besturen voorgelegd aan de leden van de betrokken beroepsverenigingen. Hiervoor wordt de concepttekst voor een bepaalde periode, ten minste 6 weken, opengesteld voor commentaar via een ingang op de SWAB-website, met de mogelijkheid om individueel commentaar te geven en amendementen toe te voegen. Het is de taak van de voorbereidingscommissie om de beroepsgroepen te stimuleren om een actieve bijdrage te leveren.
- Na genoemde raadpleging wordt de definitieve richtlijn door de voorbereidingscommissie vastgesteld. De commissie Richtlijnen van de SWAB verifieert of de procedures correct zijn verlopen en of de ingekomen commentaren naar behoren zijn verwerkt en beantwoord. Indien zij positief adviseren wordt de richtlijn door het SWAB-bestuur bekrachtigd.
- De definitieve SWAB-richtlijn met de onderliggende systematische review wordt (in het Nederlands of Engels) kosteloos beschikbaar gemaakt op de SWAB-website (http://www.swab.nl/richtlijnen). De ontvangen commentaren op de conceptrichtlijn, en de reactie van de commissie daarop worden ook op de SWAB website geplaatst.
Verspreiding en implementatie
De definitieve SWAB-richtlijn met de onderliggende systematische review wordt (in het Nederlands of Engels) kostenloos beschikbaar gemaakt op de SWAB-website (https://swab.nl/nl/richtlijnen-swab). Gestreefd wordt de (vertaalde) review, en/of een samenvatting van de richtlijn, ter publicatie aan te bieden. De SWAB houdt contact met de antibioticacommissies en zendt de richtlijnen rechtstreeks toe aan de commissies. De adviezen van de richtlijnen worden verwerkt in het Nationale Antibioticaboekje van de SWAB: SWAB-ID (www.swabid.nl). Elk ziekenhuis in Nederland kan tegen een geringe vergoeding een licentie krijgen voor een lokale versie van het Nationale Antibioticaboekje. Updates in het Nationale Boekje worden automatisch gedistribueerd naar de lokale versies, wat bevordert dat de lokale boekjes de meest recente richtlijnen volgen.
Rol van de sponsor
De inkomsten van de SWAB bestaan uitsluitend uit subsidies van het RIVM/CIb. Deze heeft geen invloed op de inhoud van de richtlijnen. Dit wordt bij elke richtlijn als zodanig vermeld.
Conflicterende belangen
De commissie richtlijnen realiseert zich dat er tussen leden van de voorbereidingscommissies en de (farmaceutische) industrie op velerlei vlak banden kunnen bestaan, welke potentieel van invloed kunnen zijn op de conclusies van de richtlijnen. De commissie volgt in het onderstaande de politiek van het British Medical Journal,7 en de Cochrane Collaboration Policy on Commercial Sponsorship,8 voorzover van toepassing.
- Bij het instellen van een voorbereidingscommissie worden vooraf conflicterende belangen geïnventariseerd, volgens het format zoals gehanteerd door de Federatie Medisch Specialisten.
NB Dit geldt ook bij de commissie die het Nationale antibioticaboekje SWAB-ID voorbereidt en onderhoudt. - Als er tijdens het proces van richtlijnontwikkeling bij een commissielid één van genoemde belangen ontstaat, meldt hij/zij dat aan de voorzitter.
- Voorzitter en coördinator mogen geen banden hebben met een bedrijf of andere partij die belangen heeft bij de richtlijn.
- Het is niet toegestaan dat één bedrijf of belanghebbende partij banden heeft met de meerderheid van de commissieleden.
- De conflicterende belangen worden gepubliceerd bij review, richtlijn en op de website.
Geldigheidsduur
De SWAB streeft ernaar de richtlijnen in principe elke 5 jaar te herzien. Tot een eerdere herziening kan door de Commissie Richtlijnen en/of het SWAB bestuur worden besloten op grond van ontwikkelingen in de wetenschap. In dat geval wordt de richtlijncommissie opnieuw bijeengeroepen. In voorkomende gevallen kan ook een Addendum gemaakt worden bij een nog geldige richtlijn.
Anderzijds kan een latere herziening worden toegestaan als er volgens de experts in het land geen belangrijke wijzigingen zijn geweest in de 5 jaar na het verschijnen van de richtlijn. In dat geval wordt de geldigheidsduur, op voorstel van de Richtlijncommissie, door het SWAB bestuur met maximaal 5 jaar verlengd.
Referenties
- Kwaliteitsinstituut voor de gezondheidszorg CBO. Handleiding voor werkgroepleden, 2000. P 18-27
- Brouwers MC, Kho ME, Browman GP, et al. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ : Canadian Medical Association journal = journal de l'Association medicale canadienne 2010; 182: E839-42.
- Pappas PG, Kauffman CA, Andes DR, et al. Clinical Practice Guideline for the Management of Candidiasis: 2016 Update by the Infectious Diseases Society of America. Clin Infect Dis 2016; 62: e1-e50.
- Guyatt GH, Oxman AD, Vist GE, et al. GRADE: an emerging consensus on rating quality of evidence and strength of recommendations. BMJ (Clinical research ed) 2008; 336: 924-6.
- McMurray JJ, Adamopoulos S, Anker SD, et al. ESC guidelines for the diagnosis and treatment of acute and chronic heart failure 2012: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association (HFA) of the ESC. European journal of heart failure 2012;14:803-69.
- Alexander PE, Gionfriddo MR, Li SA, et al. A number of factors explain why WHO guideline developers make strong recommendations inconsistent with GRADE guidance. Journal of clinical epidemiology 2016;70:111-22.
- Smith R. Beyond conflict of interest. Br Med J 1998; 317:291-292.
- http://community.cochrane.org/editorial-and-publishing-policy-resource/ethical-considerations/conflicts-interest-and-cochrane-reviews
Bijlage 1: Belangenverklaring
Bijlage 2: Format standaard formuleringen SWAB richtlijn
